Tất cả chuyên mục

Ngày 2/7, đã có gần 500 loại thuốc, vaccine sản xuất trong nước được Bộ Y tế cấp mới, gia hạn giấy đăng ký lưu hành.
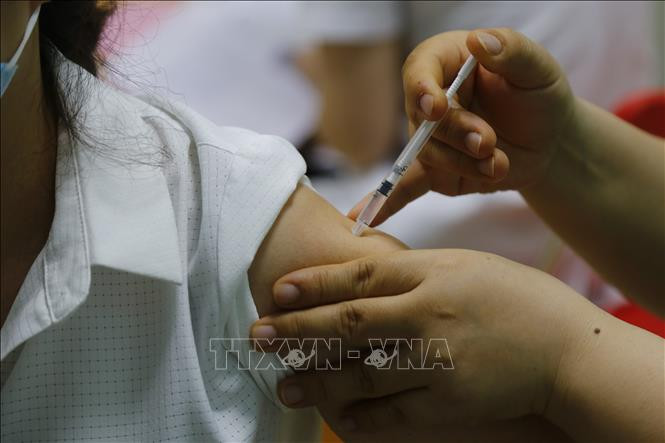
Từ đầu năm đến nay đã có trên 10.000 sản phẩm sản xuất trong nước, nhập khẩu được Bộ Y tế cấp mới, gia hạn để phục vụ mua sắm, đấu thầu cho phòng chống dịch và chữa bệnh... Mới đây nhất, ngày 2/7, đã có gần 500 loại thuốc, vaccine sản xuất trong nước được Bộ Y tế cấp mới, gia hạn, trong đó có 111 loại thuốc cấp mới và 374 thuốc gia hạn. Trong số gần 500 loại được cấp mới, gia hạn theo Luật Dược 2016 lần này có cả các thuốc được cấp mới, gia hạn trong 3 năm, có loại 5 năm.
Riêng trong tháng 6/2024, Bộ Y tế đã có nhiệt đợt gia hạn/cấp mới giấy đăng ký lưu hành khoảng trên 2.000 loại thuốc, vaccine và sinh phẩm y tế. Như vậy, đến nay đã có trên 10.000 loại thuốc, vaccine được Bộ Y tế cấp mới, gia hạn theo quy định của Luật Dược 2016.
Bộ Y tế cho biết, thực hiện Nghị quyết số 80/2023/QH15 của Quốc hội, Bộ Y tế đã có 14 đợt công bố gia hạn hiệu lực giấy đăng ký lưu hành thuốc, nguyên liệu làm thuốc đến hết ngày 31/12/2024 với tổng số thuốc, nguyên liệu làm thuốc được công bố là: 13.202 (10.301 thuốc trong nước, 2.656 thuốc nước ngoài, 245 vaccine, sinh phẩm).
Bên cạnh đó, trong năm 2023 và 5 tháng đầu năm 2024, Bộ Y tế đã cấp trên 11.000 đơn hàng nhập khẩu thuốc, nguyên liệu làm thuốc.
Các sản phẩm thuốc, nguyên liệu làm thuốc, vaccine được cấp mới, gia hạn giấy đăng ký lưu hành đều là những thuốc thiết yếu, khá đa dạng về nhóm tác dụng dược lý gồm thuốc điều trị ung thư, tim mạch, tăng huyết áp, đái tháo đường, thuốc kháng virus, thuốc điều trị bệnh lý đường hô hấp, thuốc kháng sinh, hạ sốt, giảm đau, kháng viêm thông thường khác...
Đối với các loại vaccine, sinh phẩm y tế được công bố cấp mới, gia hạn giấy đăng ký lưu hành đều là những sản phẩm có nhu cầu sử dụng nhiều trong khám chữa bệnh, phòng chống dịch bệnh...
Liên quan đến đăng ký, gia hạn lưu hành thuốc, nguyên liệu làm thuốc, tại dự thảo Luật Dược sửa đổi, bổ sung, Ban soạn thảo đề xuất quy định các trường hợp gia hạn, thay đổi, bổ sung Giấy đăng ký lưu hành không phải thông qua Hội đồng tư vấn cấp Giấy đăng ký lưu hành thuốc, nguyên liệu làm thuốc hoặc không phải phê duyệt để đơn giản hóa thủ tục hành chính.
Đồng thời, giảm thời gian giải quyết hồ sơ thay đổi, bổ sung chỉ cần công bố từ 3 tháng xuống còn 15 ngày làm việc; giảm thời hạn cấp Giấy đăng ký lưu hành từ 12 tháng xuống còn 9 tháng trong trường hợp thừa nhận, tham chiếu nhằm đẩy nhanh quá trình cấp phép, bảo đảm quyền tiếp cận thuốc sớm của người dân.
Ban soạn thảo cũng đề xuất bổ sung quy định cho phép cơ sở được tiếp tục sử dụng Giấy đăng ký lưu hành sau khi hết hiệu lực và đã nộp hồ sơ gia hạn theo quy định đến khi được gia hạn hoặc có văn bản của Bộ Y tế; bổ sung quy định cho phép thay thế CPP bằng giấy tờ pháp lý chứng minh thuốc được cấp phép trong trường hợp đáp ứng nhu cầu phòng, chống dịch bệnh…
Dự thảo luật quy định mở rộng một bước quyền phân phối thuốc của các FIE như quyền bán, giao nhận, vận chuyển thuốc, nguyên liệu làm thuốc do chính cơ sở sản xuất, đặt gia công, chuyển giao công nghệ tại Việt Nam...
Ý kiến ()